
Bessere Diagnose dank Exomsequenzierung
Exomsequenzierungen, also Analysen des proteinkodierenden Genoms, ermöglichen die sichere Identifizierung von Kindern mit Krebsprädispositionssyndrom (KPS), also seltenen Erbkrankheiten, die mit einem erhöhten Krebsrisiko einhergehen.
Mediziner um Ines Brecht vom Universitätsklinikum Tübingen suchten in 103 Kindern mit KPS und malignen oder Borderline-Tumoren mittels Exomsequenzierung nach wahrscheinlich pathogenen und pathogenen Gen-Varianten ( LP-/P-Varianten), die mit dem KPS assoziiert sind. Ihre Ergebnisse stellten sie jetzt auf dem Kongress für Kinder- und Jugendmedizin in Mannheim vor.
Die häufigsten onkologischen Diagnosen der Studienkohorte waren Leukämien (26,2%, n = 27), Neuroblastome (11,7%, n = 12), Sarkome (11,7%, n = 12), Tumoren des zentralen Nervensystems (9,7%, n = 10), Lymphome (8,7%, n = 9) und Nephroblastome (6,8%, n = 7). 7,8% (n = 8) der Studienkohorte erkrankten an mehr als einer Krebserkrankung. Bei 18,4% der Kinder identifizierten die Mediziner eine Genvariante, die für eine Krebserkrankung prädisponiert. In 13,6% der Fälle war diese die Ursache für den Krebs. Die häufigsten neu diagnostizierten LP-/P-Varianten betrafen die Gene TP53 (n = 3), PHOX2B (n = 2), NF1 (n = 2), PTEN (n = 2). Bei 29,1% (n = 30) der Studienteilnehmer fanden sie Varianten unklarer Signifikanz ( VUS).
Die Kriterien für eine genetische Beratung erfüllten 62,1% (64/103) der Studienteilnehmer. Bei 28,1 % (18/64) von ihnen ließ sich im Rahmen der genetischen Diagnostik ein KPS nachgeweisen. 36,8 % (7/18) der Studienteilnehmer mit KPS zeigten eine auffällige Familienanamnese. Nur einer der Studienteilnehmer mit KPS erfüllte keine Jongmans-Kriterien.
Die Autoren empfehlen auf dieser Datenbasis, die Sequenzierung proteinkodierender Gene in den klinischen Alltag zu integrieren, um ein besseres individualisiertes klinisches Management dieser Patienten und die prädiktive Testung von Hochrisikofamilienmitgliedern zu ermöglichen.

 immatics GmbH / Max Lautenschläger
immatics GmbH / Max Lautenschläger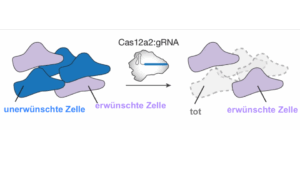 Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4
Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4 Biontech SE
Biontech SE